【鄭智文藥師】漫漫新藥路 (上)
隨著醫療科技的進步,能夠透過分子醫學更瞭解疾病,期盼新藥有較少副作用、能夠降低住院治療時間、改善生活品質、延長壽命,但現今一個新藥的誕生是逐漸困難的,從新藥探索到上市需要10-15年,根據2014年美國塔夫茨藥物研究研究中心(Tufts Center for the Study of Drug Development)的報告,統計1997年至2007年間進行初次臨床試驗的藥物,平均開發一個處方新藥的費用為26億美元,折合台幣超過800億元,然而迪馬西博士(Joseph A. DiMasi)在2016年研究 發現研發成本以8.3%年增長率增加,所以新藥研發是既昂貴又耗時的過程。

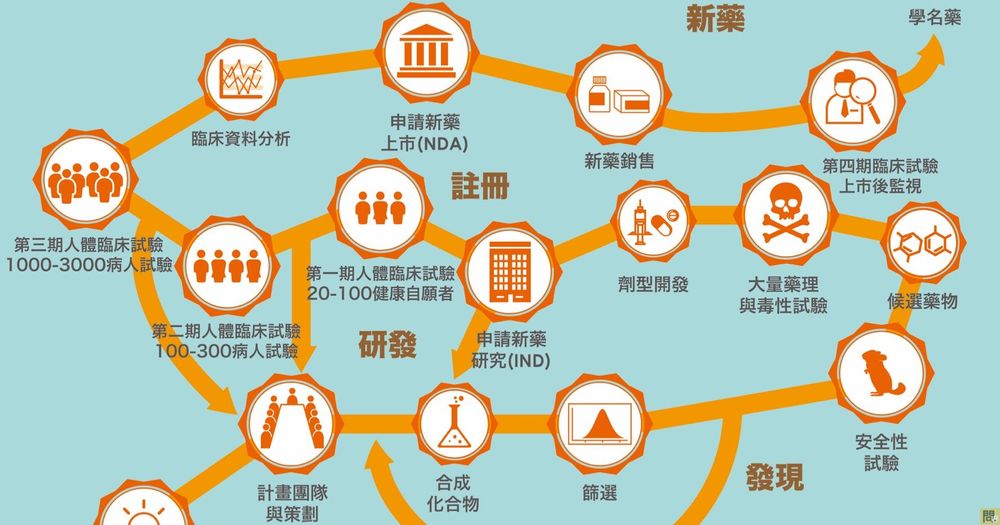
何謂新藥?新藥研發上市流程?
新藥是指新成分、新療效、新複方、新使用途徑之藥品。新藥研發上市流程可分為6個階段:新藥探索、臨床前期動物試驗、新藥審查(IND)、臨床試驗、新藥查驗登記(NDA)、上市後研究。每一階段所需投入的資金、時間,以及成功率都不相同。在研發過程中越靠前面階段,則成功率越低,風險越大;而新藥的價值,越靠近上市則價值越高,藥廠訂定價值不是基於成本,而是基於藥物對患者的價值。
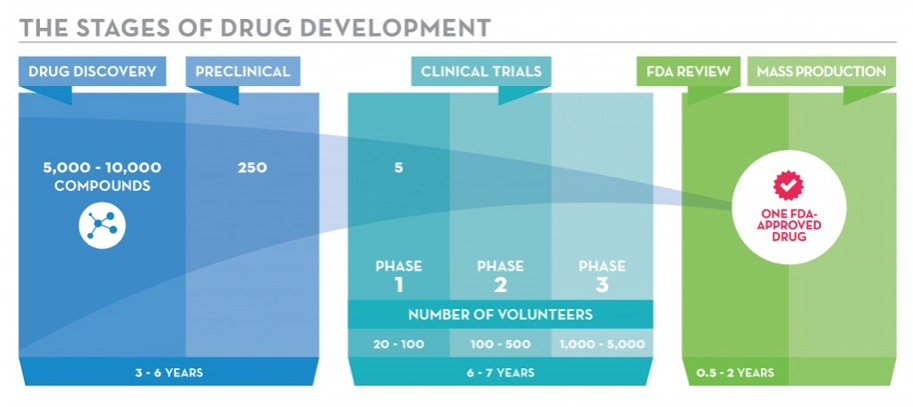
新藥的開始來自於實驗室,研究人員與科學家努力分解疾病的組成部分,以了解身體發生的異常事件或過程,然後在自然界或者運用生物技術,找到能夠對抗疾病的分子,通常是分子化合物、蛋白質藥物及植物中草藥。科學家經由試管與培養基的離體試驗到生物體內的活體試驗,以確定哪些化合物會對疾病產生某種化學作用,並瞭解候選藥物的藥理療效、生理反應、副作用與毒性反應等有效性與安全性之依據,才能向衛生主管機關提交新藥申請(investigational new drug, IND)以進行人體臨床試驗。臨床試驗前的研究過程可能需要3-6年的時間,在這段時間裡研究人員已經想好最終產品樣貌,藥物藉由什麼途徑進入人體進行治療,還必須考慮藥物的組成配方,專利申請時程以及如何讓藥物容易生產與製造。
新藥申請之審查必須確保新藥的品質與嚴謹度,有效率的審查制度才能爭取時效,避免延宕研發進度。美國與日本對於新藥申請臨床試驗的安全性審查為30天,歐盟法令規定最多60天,台灣目前平均是79天。在衛生主管機關核准之後才能進行臨床試驗的三個階段。
罕見疾病是指罹病患者少、疾病盛行率低的疾病,常常受限於市場與成本的考量,導致研究與開發注入的意願低。治療罕見疾病的藥物即為孤兒藥(Orphan drug),取自孤兒孤苦無依、無人重視的意思,各國對於罕見疾病藥物都有相對應的政策與優惠措施,若在美國新藥申請過程取得孤兒藥資格(Orphan drug designation, ODD),政府會提供研發補助,並享有行政上的審查彈性與上市後七年獨賣期,大幅增加了藥廠對於孤兒藥研發的興趣。
新藥臨床試驗三階段
臨床試驗,必須提供能確認其療效及安全性之臨床試驗報告,作為核准上市的重要依據。臨床試驗的執行都應該在衛生主管機關核可之醫學中心或醫院執行,而且必須經過人體試驗倫理委員會(Institutional Review Board, IRB)之同意,確保受試者被詳細告知所有風險與權益而同意參與,以符合優良臨床試驗規範(Good Clinical Practice, GCP)。
臨床試驗第一期是以20-100位健康受試者進行安全性試驗。研究人員能測量出藥物動力學(pharmacokinetics)與藥效學(pharmacodynamics)之參數,看看藥物在人體吸收、分佈、代謝、排除之經時變化,找出人體對藥物最高耐受劑量範圍(maximum tolerated dose)、所發生的副作用,以瞭解藥物在人體裡的表現。第一期通常需要半年至一年時間完成。
臨床試驗第二期是以100-300位(或更多)患有疾病的患者進行安全性與有效性試驗。因為此期的藥物會在更廣泛的族群中進行測試,因此可以更加了解藥物潛在安全性的疑慮。患者會與不同的治療方式或安慰劑做比較,以決定最佳劑量、用法與給藥間隔,將在之後的第三期臨床試驗中進行驗證。第二期通常需要約二年的時間完成。
臨床試驗第三期是在藥物被批准上市前的最後驗證性研究,通常被稱為樞紐試驗(pivotal studies)。是以1000-3000位(或更多)患者進行大規模的隨機、雙盲、對照之試驗,可能在多國、多地區的多個醫學中心執行,是最耗費、最耗時、最耗力的臨床試驗階段。研究人員會定期密切監測病患,以確認藥物的療效,證明新藥的不劣性(non-inferiority),即療效至少能達到與現有藥物的水準,並收集更多關於藥物的副作用,確保正確使用藥物方式。第三期通常需要三年的時間完成,現在無論是台灣或者美國藥證申請都需要樞紐試驗12周,與開放性延伸試驗40周之有效性與安全性的統計資料才能夠申請藥證。

杏隆藥局 諮詢藥師
問8 線上視訊諮詢
諮詢專業醫師的第二意見,確保您得到最適合的治療方案
您可能想知道
追蹤問8粉絲專頁




